Forum für Lebensverlängerung
»
Radikale Lebensverlängerung, Sport, Verschiedenes
»
Radikale Lebensverlängerung
»
Senolysis, Reloaded
Forum für Lebensverlängerung
»
Radikale Lebensverlängerung, Sport, Verschiedenes
»
Radikale Lebensverlängerung
»
Senolysis, Reloaded


|
|
Senolyse, von mir noch einmal neu gedacht. |

|
|
Wir sollten dringend eine genauere Vorstellung davon entwickeln, wie Seneszente Zellen normalerweise "verschwinden". |

|
|
Zunächst einmal ist es aber in jedem Fall wichtig, dass der Köper die SPMs überhaupt produzieren kann.
Dr.Faust sagt danke
|

|
|
Und nicht zuletzt sollten wir uns einmal genau ansehen, wie genau die seneszenten Zellen von einem funktionierenden Immunsystem zerstört werden können. |

|
|
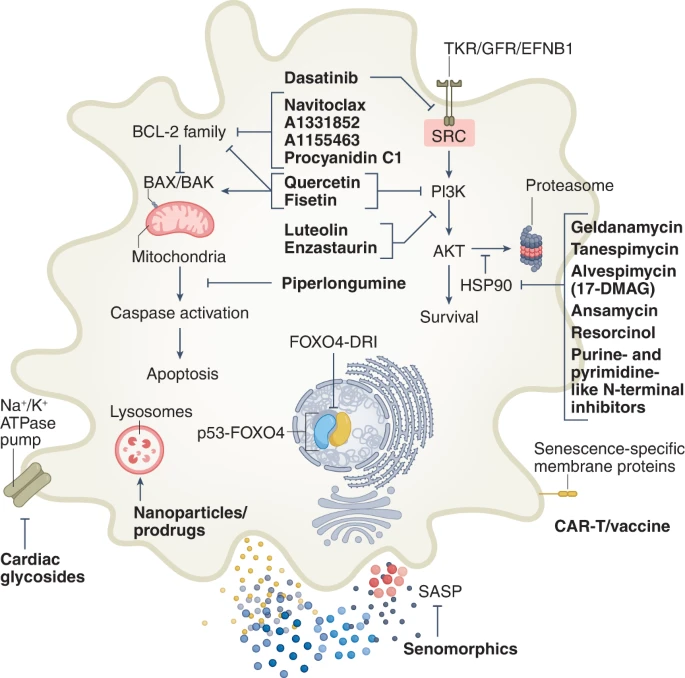
Hier eine übersichtliche Grafik zu den uns bekannten Senolytika:
Roger sagt danke
|

|
|
Eine weitere bislang kaum beachtete Option gegen seneszente Zellen ist das Blocken von endogenen Retroviren!
Dr.Faust sagt danke
|

|
|
Sehr interessant und sehr aussagekräftig in Bezug auf Entstehung von neuen Viren usw. usf. |

|
|
Zunächst einmal muss man sehen, was überhaupt blockiert werden soll!
Dr.Faust und Methusalem haben sich bedankt!
|

|
|
Zitat von Methusalem im Beitrag #7 Grundsätzlich gilt: Eine Blockade macht nur Sinn, wenn HML-2 bereits aktiviert ist. In früheren Stadien der Alterung wäre eher eine Prävention der HML-2 Aktivierung vorrangig! Im Prinzip lohnt es sich, im Nachbarthread Retrotransposon (5) vorbeizuschauen, ich denke dass einiges, was für das LINE-1 Retrotransposon zutrifft auch bei HML-2 hilfreich sein könnte, zum Beispiel indem man die im Alter auftretenden genomweiten Hypomethylierungen eindämmt (durch einen sauberen circadianen Rhythmus und Vermeidung von chronisch erhöhten Cortisol-Signalling etc). Bei einer spezifischen Blockade von HML-2 wird von Forschenden in der Regel "klassisch" mit antiretroviralen Medikamenten gearbeitet, z.B. hier . In der Publikation #6 wurde HML-2 mit einer spezifischen shRNA geblockt. Ich denke aber, dass das noch nicht der Weisheit letzter Schluss ist. Im Prinzip sollte eine funktionierende Senolyse bereits einen Teil der Zellen eliminieren die HML-2 aktiviert haben und somit einen nachhaltigen Effekt gegen das Inflam-Aging erzielen können. |

|
Gelöschtes Mitglied

|
Clearance of defective muscle stem cells by senolytics restores myogenesis in myotonic dystrophy type 1 Zitat
Tizian und Prometheus haben sich bedankt!
|

|
|
Zitat von version2 im Beitrag #10
Zitat
|

|
Gelöschtes Mitglied

|
Ich sehe das inzwischen auch so wie du(?), dass man besser die körpereigenen Mechanismen nutzen sollte, da verschiedene Zelltypen unterschiedlich auf Senolytika zu reagieren scheinen. Insofern vorstellbar, dass man durch Supplementierung von Senolytikum für Zelltyp X unbeabsichtigt auch gesunde Zellen des Typs Y killt.
Prometheus sagt danke
|

|
|
Ja, nach aktuellem Stand ist es nahezu unmöglich, vorab die korrekte Dosierung eines Senolytikums zu berechnen.
Roger sagt danke
|

|
Gelöschtes Mitglied

|
Zitat von Prometheus im Beitrag #13 Gibt es da irgendwelche Forschung zu? Für mich klingt wenigstens die erste Behauptung unrealistisch, denn warum gibt es sonst 1-2 wöchige Fastenkuren? Ketose sollte man ja spätestens nach 3-4 Tagen erreicht haben, wenn ich mich nicht komplett versehe. Nebenbei: Würde ich nochmals Senolytika nehmen, dann zu einer Zeit, in der ich mich komplett schonen kann und nicht darüber hinaus. Die Idee dahinter ist, dass gesunde Zellen, die aus welchem Grund auch immer erhöhtem Stress ausgesetzt sind, nicht auch weggemacht werden sollen. |

|
|
Zitat
|

|
|
Aber so viel länger leben Teetrinker auch nicht oder sehen faszinierend jung aus. Würde es glaubhafte Studien zu den ganzen Giften auf diesen Monokulturen geben, so denke ich, wäre der Nutzen von Tee und Kaffee eher ein Minus. |

|
|
@Illuminatus Zitat
Illuminatus und Roger haben sich bedankt!
|

|
|
Seneszente Melanozyten (Pigmentzellen), wie sie beispielsweise in Muttermalen vorkommen, sollten auf eine senolytische Behandlung reagieren. Zitat
Zitat
Illuminatus und Roger haben sich bedankt!
|

|
Gelöschtes Mitglied

|
Zitat von Prometheus im Beitrag #17Zitat
Prometheus sagt danke
|

|
|
@version2 Zitat
|

|
|
Back to topic: Zitat
|

|
Gelöschtes Mitglied

|
Senolytics in Aging Muscle: Could the Cure Be Worse than the Disease? Zitat
Prometheus sagt danke
|

|
|
Genome-wide CRISPR activation screening in senescent cells reveals SOX5 as a driver and therapeutic target of rejuvenation
Prometheus sagt danke
|

|
|
Zitat von Speedy im Beitrag #23 Ja, und auch hier wieder: Was den Stammzellen gut tut, kann auch für Krebsstammzellen förderlich sein: SOX5 promotes cell invasion and metastasis via activation of Twist-mediated epithelial–mesenchymal transition in gastric cancer https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6452794/ Trotzdem sehr interssant....Welche SOX5 Aktivatoren gibt es?
CRONos sagt danke
|

|
|
|

 Thema drucken
Thema drucken 02.02.2023 19:43 (zuletzt bearbeitet: 02.02.2023 20:30)
02.02.2023 19:43 (zuletzt bearbeitet: 02.02.2023 20:30)

 Antworten
Antworten